Autor: Sergio Ollero Sánchez
Graduado en Enfermería por la Universidad de Barcelona (UB)
El plasma es un liquido transparente y ligeramente amarillento que representa el 55% del volumen total de sangre. En él se encuentran suspendidas las células sanguíneas tales como glóbulos rojos, glóbulos blancos y plaquetas. Está formado por agua en un 90%, sales minerales y una gran cantidad de proteínas que velan por el buen funcionamiento de nuestro organismo entre las que destacan: inmunoglobulinas (que nos defienden ante infecciones), factores de coagulación (que junto con plaquetas ayudan a detener sangrados) y albumina (proteína transportadora de hormonas y fármacos hasta tejidos).
Las plaquetas o trombocitos no son más que partículas ovoides, irregulares sin núcleo ni otros orgánulos. Se originan en la médula ósea y tienen una vida media de 7 a 10 días desde que son liberadas al torrente sanguíneo, donde encontramos 2/3 partes del total, ya que el resto se almacena en el bazo.
Las plaquetas, además de ser esenciales para la coagulación, participan en la reparación del tejido lesionado, gracias a los factores de crecimiento plaquetario presente en estas, mediadores biológicos que regulan los procesos de regeneración y reparación tisular.
Después de una lesión se producen cambios en las plaquetas, que afectan su morfología y bioquímica, activándolas. Una vez activadas se van destruyendo, y durante este proceso liberan importantes sustancias coagulantes que conducen a la formación de un tapón hemostático, siendo este el primer paso de la cicatrización.
Además de estar implicadas en la hemostasia por su función pro-coagulante, son fuente natural de varios Factores de Crecimiento involucrados en vigilar la continuidad de los vasos sanguíneos y en la reparación de tejidos. Actúan como vehículo de estos factores de crecimiento y los liberan en las zonas donde hay daño tisular.
Los factores de crecimiento son proteínas con un papel clave dentro del complejo proceso de bioestimulación, reparación y regeneración tisular.1
El concepto de PRP (Plasma Rico en Plaquetas) comenzó en la década de los 70, en el campo de la hematología para tratar a pacientes con trombocitopenia mediante trasfusiones. Una década después comenzó a llegar a otros ámbitos de la medicina.
Mas recientemente comenzó su uso en estética debido a sus propiedades regeneradoras, cicatrizantes, rejuvenecedoras y en alopecia. Se ha observado en diferentes estudios que el PRP puede estimular la proliferación de fibroblastos e incrementar la síntesis de colágeno tipo I, además de aumentar la formación de tejidos blandos subcutáneos y mejorar la calidad de la piel.
El PRP es un producto biológico, definido como una porción de plasma con una elevada concentración de plaquetas.2
El PRP contiene al menos 6 grandes factores de crecimiento, que promueven 4 acciones principales en el medioambiente local : Proliferación, Migración, Diferenciación celular y Angiogénesis. Estos factores son:
PDGF (Factor de crecimiento derivado de las plaquetas): Promueve indirectamente la angiogénesis a través de los macrófagos, activa los macrófagos, promueve la proliferación de células adiposas y de los fibroblastos dérmicos, facilita la formación de colágeno tipo I A nivel piloso controlaría el folículo piloso así como su vascularización.
TGF (Factor de crecimiento transformante): Inhibe la formación de osteoclastos, promueve la proliferación y diferenciación de las células mesenquimales, promueve la quimotaxis, angiogénesis y síntesis de colágeno A nivel piloso estimularía la foliculogénesis y su maduración.
EGF (Factor de crecimiento epidérmico): Induce la migración celular, estimulan la formación de tejido de granulación A nivel piloso mejoraría la actividad del crecimiento en la raíz folicular.
FGF (Factor de crecimiento fibroblástico): Promueve la proliferación de los fibroblastos e índice la secreción de fibronectina, inhibe osteoclastos, estimula y coordina la mitogénesis de las células mesenquimales, promueve la angiogénesis A nivel piloso mejoraría el avance de los folículos
IGF (Factor de crecimiento insulina-like): Promueve la proliferación y diferenciación de células mesenquimales y de revestimiento, estimula la síntesis de osteocalcina, fosfata alcalina y colágeno tipo I, actúa como agente quimotáctico para células vasculares endoteliales A nivel piloso incrementaría la densidad del pelo e inhibe la apoptosis , además de mejorar la migración y supervivencia de las células pilosas
VEGF (Factor de crecimiento vascular endotelial): Promueve la hiperpermeabilidad de los vasos sanguíneos, promotor de la quimotaxis y diferenciación de las células epiteliales, renales, gliales y de fibroblastos A nivel piloso mejoraría la microvascularaización peri folicular.3Actualmente existe gran discusión y falta de consenso en la preparación del PRP., aunque el concepto es el mismo: obtener sangre, añadir un anticoagulante, centrifugar y por último añadir o no un activador como podría ser el calcio. Existen 2 técnicas:
Técnica abierta: El producto es expuesto al ambiente del lugar de trabajo y entra en contacto con diferentes materiales, como pipetas, tubos de ensayoetc. Existe riesgo de contaminación del producto, pese a que es la técnica más utilizada.
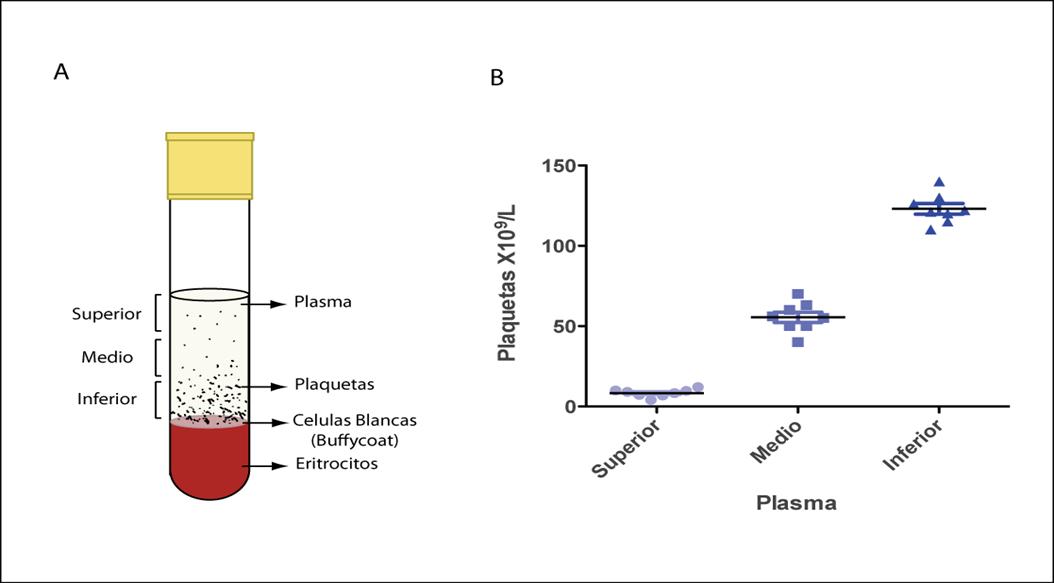
Técnica cerrada: Es la realizada mediante la utilización de productos comerciales “Kits”, que incluyen productos de centrifugación en el cual el producto no esta expuesto al medioambiente de trabajo. Siendo este método el más recomendado, aunque posiblemente el más caro.2La obtención del PRP suele ser sencilla, mediante una extracción de sangre del paciente, extraída por venopunción, generalmente la zona preferente de elección para extraer la muestra será una vena del antebrazo, indiferentemente la basílica, cefálica o mediana del codo, debido a su acceso más fácil (ver foto), a un tubo con anticoagulante, los más utilizados Citrato de Sodio o ACD (Acid Citrat Dextrose), ninguno de los dos ha mostrado ventajas respecto al otro. A continuación se centrifuga la muestra. Después de la centrifugación el tubo muestra 3 zonas bien delimitadas, abajo del todo la serie roja, los eritrocitos; justo por encima una fina capa llamada “BufyCoat” donde quedan los leucocitos o serie blanca y justo por encima quedaría el plasma rico en plaquetas. Aunque cabe mencionar que la concentración de plaquetas no es la misma a lo largo de todo el volumen de plasma. Se ha observado que la concentración de las plaquetas es diversa en el plasma, no es uniforme, aumentando su concentración hacia las capas más bajas del plasma, de donde viene el nombre de plasma rico en plaquetas (PRP), el cual constituye aproximadamente 2/3 del volumen de plasma.
El uso de anticoagulantes puede modificar la estructura de las plaquetas haciendo que estas se hinchen, tomando forma esférica, perdiendo su forma discoidea. Para la obtención de PRP se utiliza el citrato de sodio o ACD como anticoagulante, con el fin de no dañar ni alterar las propiedades de las plaquetas.
La presencia de leucocitos y neutrófilos, esta en entre dicho, algunos autores afirman que puede repercutir negativamente en la formación de la fibrina autóloga, además de interferir en la agregación plaquetaria, además de que las citoquinas pro inflamatorias pueden expresar metal proteínas capaces de degradar la matriz extracelular. Sin embargo otros autores afirman lo contrario.
Lo mismo ocurre con las plaquetas, no se ha demostrado que cuanto mayor sea la concentración de plaquetas en el PRP mejor efecto tendrá, incluso algunos autores comentan que un exceso de plaquetas podría tener un efecto contraproducente.
Se debe tener en cuenta que el volumen de plasma varía entre pacientes, y como resultado, el volumen de PRP que se obtiene de 40mL de sangre, volumen más habitual que se extrae de muestra del paciente, también varía entre pacientes.
La obtención de PRP, tal y como hemos comentado, sea cual sea la técnica utilizada, se debe realizar en condiciones de total esterilidad.
La activación de las plaquetas presente en el PRP, tradicionalmente, se induce de forma fisiológica a través Ca2+. El calcio se proporciona a través de una solución de cloruro de calcio concentrada (100 mg/mL), que se le añade al PRP para lograr una concentración final de 10 mg/mL, o sea el volumen a añadir representa el 10% del volumen de PRP obtenido e inmediatamente se inicia su aplicación, aunque también se puede activar mediante trombina o no activarlas; ya que no existe evidencia de que es mejor.
Además también se podría añadir otras sustancias que potencien o mejoren la calidad del PRP como seria el caso de Biotina, progesterona (para inhibir la acción de la 5-alfa-reductasa que convierte la testosterona en dehidrotestosterona, responsable de la alopecia en numerosos casos) o acido hialurónico
Después de su preparación el PRP es estable en condiciones de anticoagulación durante unas 8 horas, sin embargo una vez activadas las plaquetas ha de aplicarse antes de 10 minutos.1
La acción del PRP comienza muy rápido, desde su administración, ya que entre el quinto y séptimo día el PRP atrae los macrófagos y a partir de aquí́ los procesos regenerativos serán estimulados por los factores de crecimiento derivados de estos macrófagos. Entre la segunda y tercera semana, la actuación directa de los factores de crecimiento permite la mitogénesis celular y la angiogénesis. Entre la cuarta y sexta semana se produce revascularización y regeneración celular, desaparecen los macrófagos, iniciándose un proceso restitutivo; que pretende llevar a la normalidad el metabolismo y funcionamiento cutáneo.
El PRP es una de las herramientas medicas regenerativas más novedosas. Existen varias formas de utilizar los efectos del PRP rico en factores del crecimiento en el mundo de la estética; Por ejemplo, se puede usar:
– De manera tópica por sus efectos estimuladores sobre el fibroblasto dérmico, en forma de coagulo, a modo de mascarilla tras exfoliaciones tanto químicas como físicas o tras aplicación de laser. La aplicación tópica ha demostrado reducir los signos y síntomas del envejecimiento cutáneo, incluyendo la reducción de las arrugas y la elastosis, además de provocar un incremento en la síntesis de colágeno dérmico. Provocando un incremento en el grosos de la epidermis y un aumento de la densidad de los fibroblastos en la dermis superficial.
– De manera intradérmica, mediante la mesoterapia para el tratamiento de arrugas, elastosis, discromías, alopeciasetc. Además la propia administración intradérmica , se ha manifestado como un estimulo para la producción de colágeno tipo I, por lo que tiene un valor añadido la administración de PRP mediante esta vía.
Produce cambios notables ya que restaura vitalidad cutánea, aumenta grosor de la piel, recupera la consistencia elástica de la piel, mejora la afluencia vascular, estimula las secreciones y mejora la tersura y apariencia de la piel.3
Además según donde y como lo apliquemos podremos conseguir una disminución de la profundidad de los ojos, disminución de la profundidad del surco naso geniano, elevación de la cola de la ceja, disminución de las arrugas transversales de expresión, disminución de código de barras en labio superior, disminución de la rectitud y angulación de los labios, mayor suavidad en la expresión del rostro, mejor armonía, mejor homogeneidad de las discromías.
En estrías si al PRP le añadimos tratamientos de radiofrecuencia , laser y ultrasonidos, obtenemos mejores resultados.
En manchas de la piel, si lo combinamos con laser y microneedeling también se consiguen excelentes resultados.
Por no hablar de los buenos resultados obtenidos en el tratamiento de las alopecias. Aunque no se entiende bien el mecanismo por el cual el PRP funciona en el tratamiento de la alopecia, diferentes autores están de acuerdo que incrementa la vascularización, previene la apoptosis y la fase catágena, prolonga la duración de la fase anágena del folículo piloso, además de acelerar la transición de la fase telógena a la anágena.
Incluso, se están realizando estudios para ver su viabilidad en pacientes que han recibido radiación, para ver si administrando PRP de forma profiláctica se consigue que la piel se dañe menos después de su exposición a la radiación.4
La combinación de PRP con cualquier otra técnica estética, ha demostrado mejoras sustanciales en todos sus ámbitos, ya que potencia dichas otras técnicas.5
El uso de materiales autólogos en el rejuvenecimiento cutáneo facial es recomendado ya que, su obtención es fácil y de bajo coste, el riesgo de rechazo (granulomas) por incompatibilidad es mínimo, las características físicas facilitan su uso al ser más manejable y moldeable, logrando un resultado final superior, debido a su aspecto natural, siendo estables y duraderos.
En el caso de Plasma rico en plaquetas no existe ningún tipo de reacción alérgica ya que se obtiene de la misma sangre del paciente, pero en ciertos casos pueden existir efectos adversos tales como:
Leves: se puede presentar eritema o hematomas locales que pueden desaparecer en 48 horas. Para evitarlo después de la inyección se puede aplicar crioterapia durante 5 minutos. También se puede registrar cefalea.
Moderados: tras la extracción de sangre, el paciente puede sentir mareos, también puede presentar hematomas en el lugar de venopunción.
Graves: el PRP tiene poca o nula morbilidad, no es necesario el reposo ni hospitalización. Puede producirse una celulitis cutánea que pueda necesitar antibióticos, debido a una posible infección por contaminación.
Algunos autores dicen que podría tener efectos cancerígenos ya que los concentrados de factores de crecimiento podrían llegar a actuar como promotores de la carcinogénesis, aunque no se ha demostrado.
El protocolo, según la técnica más usada para la obtención de PRP consiste en los siguientes pasos:
1) Selección de venas: se extrae 10-30 Ml de sangre de las venas metacarpianas o ante cubitales (vena basílica, cefálica o mediana del codo) del paciente que se realizará el tratamiento. Si la superficie que se trata es grande, mayor debe ser el contenido.
2) Anti coagulación: la sangre se deposita en tubos estériles con citrato de sodio al 3,8% o ACD para impedir la coagulación.
3) Centrifugado: según la técnica elegida abierta o cerrada , del cual se obtiene 3 fracciones:
Fracción 1: es plasma pobre en plaquetas.
Fracción 2: corresponde a plasma que contiene plaquetas en una cantidad similar que hay en la sangre periférica.
Fracción 3: es la porción más rica en plaquetas, queda justo por encima de la “Bufycoat”
4) Pipeteo de las muestras, si hemos utilizado técnica abierta: se aspira la primera fracción a un tubo estéril, se repite lo mismo con el tubo 2, la última fracción se aspira cuidadosamente, ya que es el que contiene mayor cantidad de plaquetas y para no sobrepasar la “Bufycoat” y absorber los hematíes. Posteriormente se desecha la parte de hematíes y glóbulos blancos.
5) Activación y agregación de las plaquetas mediante cloruro de calcio al 10%.
6) Aplicación del PRP en la zona a tratar antes de 10 minutos después de su activación.1
Bibliografia
Anitua E, Andia I, Ardanza B, et al: Autologous platelets as a source for healing and tissue regeneration. Thromb Haemost, 2004. 91(1): 4-15
Rubina Alves, Ramon Grimalt. A review of Platelet-Rich Plasma: History, Biology, Mechanism of Action, and Classification. Skin Appendage Disord 2018;4:18-24. DOI: 10.1159/000477353
Jordi Rodriguez Flores, Maria Angustias Palomar Gallego, Jesus Torres Garcia-Denche. Plasma Rico en plaquetas: fundamentos biológicos y aplicaciones en cirugía maxilofacial y estética facial. Rev Esp Cir Oral Maxilofac. 2012;34(1):8-17
Lucia D´Oliveria-Pazos, Juan-Manuel Fossati-Cola, Daniel-Andrés Wolff-de-Freitas, Álvaro Luongo-Gardi, Marta Otero, Beatriz Carrasco. Utilización de plasma rico en plaquetas en la profilaxis del daño cutáneo inducido por radioterapia: modelo experimental. Cir. Plást. Iberolatinam. 2016; 42(2): 109-114. DOI: 10.4321/S0376-78922016000200003
Jason Emer. Platelet-Rich Plasma (PRP): Current Applications in Dermatology. STL. 2019; 24(5)
Cursos relacionados
Postgrado enfermera gestora de la imagen corporal
Curso Online Ácido hialurónico
Curso online de dermapen
The post appeared first on Nus Agency.